Descoperire Revoluționară –
Cuprins
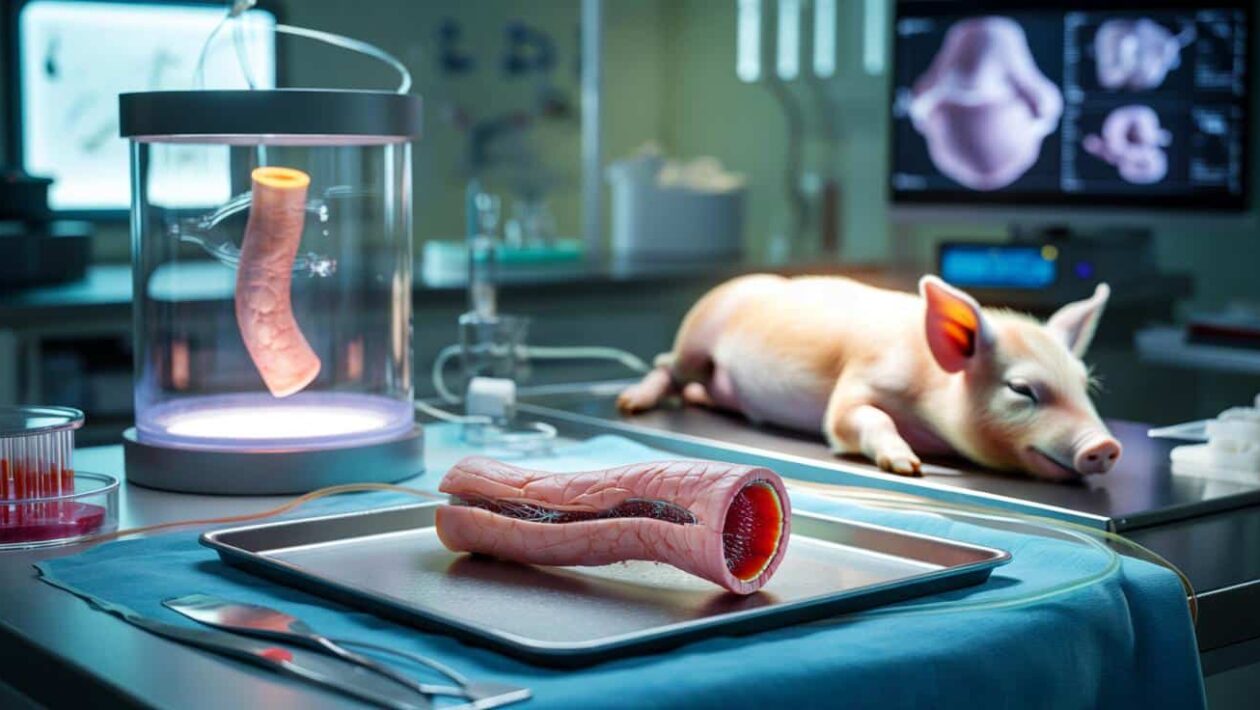
Cercetătorii au reușit să cultive în laborator o bucată de esofag provenită de la un porc, să o implanteze și să permită animalului să mănânce din nou în mod normal. Tehnica pare desprinsă direct din science-fiction, dar ar putea fi în curând absolut necesară pentru bebelușii și pacienții care se nasc fără un esofag funcțional sau care își pierd o parte din acesta.
Descoperire Revoluționară: De ce este atât de dificilă înlocuirea esofagului
Înlocuirea esofagului pare simplă: se creează un tub și se introduce în locul esofagului. În practică, însă, lucrurile nu stau așa. Esofagul:
- trebuie să împingă alimentele către stomac prin contracții musculare coordonate
- este supus unei solicitări mecanice constante prin înghițire și respirație
- conține o rețea fină de nervi și vase de sânge
În prezent, chirurgii folosesc adesea o porțiune din stomac sau din intestin pentru a înlocui o porțiune lipsă din esofag. Aceasta salvează vieți, dar noua conexiune nu este niciodată la fel ca organul original. Copiii suferă adesea de probleme de înghițire, arsuri la stomac și intervenții repetate.
Un esofag artificial viu și funcțional, care crește odată cu copilul, este considerat de ani de zile Sfântul Graal al chirurgiei pediatrice.
În special în cazul unei anomalii congenitale precum atrezia esofagiană în segment lung – în care lipsește o mare parte din esofag – medicii se lovesc de limitele tehnicilor actuale.
Cum au construit cercetătorii un esofag pe baza țesutului de porc
Echipa de cercetare condusă de chirurgul pediatric Paolo De Coppi de la University College London a optat pentru o abordare de bioinginerie. Esența acesteia: utilizarea structurii unui organ animal, dar umplerea acestuia cu celule proprii ale pacientului.
Pasul 1: „spălarea” esofagului animal
Cercetătorii au prelevat mai întâi un esofag de porc și au îndepărtat cu grijă toate celulele vii din acesta. Ce a rămas a fost doar așa-numita matrice extracelulară: un fel de schelet biologic format din proteine și fibre care păstrează forma și structura stratificată a esofagului, dar nu provoacă o reacție de respingere.
Această matrice funcționează ca un șablon natural. Straturile fine de mușchi, curbura lumenului și distribuția țesutului conjunctiv rămân intacte, în timp ce sistemul imunitar nu are motive să atace materialul.
Pasul 2: umplerea cu celule musculare proprii ale animalului
Apoi, cercetătorii au prelevat celule musculare de la viitorii recipienți: mini-porci de aproximativ zece kilograme. Echipa a reprogramat aceste celule în celule de tip stem care pot forma diferite tipuri de celule.
Încălzirea globală încetinește rotația planetei: ce impact are acest lucru asupra tehnologiei noastre
Ciuperca care te mănâncă pe dinăuntru se răspândește la nivel mondial din cauza încălzirii globale
4 fraze politicoase pentru a stabili limite fără a provoca certuri
O idee genială de Paște: cum o ramură de Paște într-o vază îți înlocuiește întreaga față de masă
Pleoape căzute după 50 de ani? Aceste 4 trucuri inteligente de machiaj îți ridică privirea
Aceste cinci clasice de la Ikea sunt cele mai apreciate de cumpărători
Aici se ascunde viespea asiatică în jurul casei tale (și așa o găsești)
De ce în aprilie este cu adevărat înțelept să deschizi ferestrele abia după ora 22:00
Aceste celule noi au fost introduse în esofagul de porc „golit”. Apoi, țesutul a fost introdus timp de o săptămână într-un bioractor, un fel de vas de cultivare de înaltă tehnologie în care:
- se administrează continuu nutrienți și oxigen
- fluxul și presiunea imită circulația sanguină reală
- stimulii mecanici ajută celulele să se organizeze
În total, procesul – de la recoltarea țesutului până la implantul final – a durat aproape două luni. Pentru copiii cu o malformație complexă a esofagului, acest lucru se încadrează în tratamentele actuale, care implică adesea mai multe operații și spitalizări îndelungate.
Operație la opt mini-porci: funcționează cu adevărat?
Testul a avut loc în timpul operației. La opt mini-porci, chirurgii au îndepărtat o bucată de esofag de 2,5 centimetri și au înlocuit-o cu segmentul cultivat în laborator.
În jurul implantului au aplicat o plasă biodegradabilă. Această înveliș temporar stimulează creșterea de noi vase de sânge în jurul transplantului, astfel încât țesutul să primească rapid nutrienți și oxigen din propriul corp al animalului.
Toate cele opt animale au trecut fără complicații majore de primele treizeci de zile cruciale după operație, o perioadă în care majoritatea transplanturilor eșuate dau greș.
Publicația din revista Nature Biotechnology menționează că cinci dintre cele opt porci au trecut cu bine de întreaga perioadă de observare de șase luni. Aceste animale:
- puteau înghiți din nou normal și se puteau hrăni singure
- aveau un segment de esofag care se contracta activ
- prezentau o rețea bine dezvoltată de nervi și vase de sânge
La unele animale au apărut îngustări în noul segment de esofag. Medicii au rezolvat aceste probleme cu tratamente endoscopice, o metodă care este obișnuită și la oameni, de exemplu după o operație la esofag sau radioterapie.
Celelalte trei porci au fost eutanasiate mai devreme din motive de bunăstare. Raportul menționează că nu a fost vorba de o singură defecțiune tehnică specifică, ci de o combinație de factori pe care cercetătorii îi analizează acum mai în detaliu.
Următorul pas: segmente esofagiene mai lungi și aplicarea la oameni
Un segment de 2,5 centimetri este mai ales o dovadă a conceptului. Copiii cu o anomalie congenitală gravă au uneori o lipsă de zece centimetri sau mai mult. Echipa din Londra lucrează acum la segmente de esofag de 10 până la 15 centimetri.
Cel mai mare obstacol: suficiente vase de sânge
Cu cât implantul este mai lung, cu atât este mai mare provocarea pentru alimentarea cu sânge. Fiecare celulă din transplant trebuie să se afle la micrometri distanță de un vas de sânge pentru a supraviețui și a funcționa corespunzător.
| Provocare | De ce este important |
|---|---|
| Vascularizare | Fără o rețea densă de vase sanguine, țesutul moare. |
| Creșterea la copii | Implantul trebuie să crească odată cu organismul, altfel apar tensiuni sau scurgeri. |
| Conexiuni nervoase | O bună coordonare a mușchilor de înghițire necesită conectarea la sistemul nervos. |
| Producție la scară largă | Pacienții au nevoie de implanturi fiabile și reproductibile, nu de teste de laborator unice. |
De aceea, cercetătorii încearcă să standardizeze cât mai mult procesul de producție. Obiectivul: un fel de „stoc” de matrice purificate din esofagul porcin, care, într-o a doua etapă, sunt umplute după dorință cu celule ale pacientului individual.
Deoarece celulele finale provin de la copilul sau adultul însuși, probabil că nu este necesară o imunosupresie puternică. Acest lucru elimină o listă considerabilă de efecte secundare și face abordarea mai atractivă pentru pacienții vulnerabili.
Ce poate însemna acest lucru pentru copii și adulți
Dacă studiile ulterioare vor avea rezultate bune, De Coppi consideră că în trei-patru ani ar putea începe un prim studiu clinic la scară mică pe oameni. Acesta s-ar concentra inițial pe copiii cu anomalii congenitale complexe ale esofagului.
Dar impactul ar putea fi mai amplu. Și adulții se confruntă frecvent cu pierderea unei părți din esofag, de exemplu în urma:
- cancerului de esofag și îndepărtării ulterioare a unei părți a organului
- ingestia de substanțe corozive, cum ar fi detergenții sau acizii
- arsuri grave la nivelul toracelui
În prezent, acești pacienți beneficiază adesea de o reconstrucție cu o porțiune de stomac sau intestin. Un segment de esofag cultivat pe măsură le-ar putea îmbunătăți calitatea vieții, cu mai puțin reflux, un comportament de înghițire mai natural și, eventual, perioade de recuperare mai scurte.
Cum funcționează bioingineria organelor
Tehnica utilizată se înscrie într-o tendință mai largă din cadrul medicinei regenerative. Cercetătorii nu mai încearcă doar să repare ceea ce este deteriorat, ci și să reconstruiască părțile lipsă pe baza propriilor celule.
Această abordare se concentrează în mare parte pe trei elemente:
- Schelet (matrice): un cadru biologic sau sintetic care conferă formă și rezistență.
- Celule: adesea celule stem proprii sau celule corporale transformate care se dezvoltă în celule musculare, nervoase sau de acoperire.
- Mediul: bioractoare care imită mișcarea, presiunea și alimentația, astfel încât țesutul să se comporte ca într-un corp real.
Tehnici similare sunt testate pentru trahee, vase de sânge și porțiuni ale intestinului. Esofagul reprezintă o provocare suplimentară, deoarece trebuie să conducă și să se contracte activ.
Ce pot face deja pacienții și părinții cu aceste cunoștințe
Pentru părinții copiilor cu anomalii ale esofagului, în prezent nu se schimbă prea multe în ceea ce privește parcursul terapeutic. Operațiile standard rămân necesare și continuă să salveze vieți. Totuși, această evoluție poate da speranță că generațiile viitoare de copii vor avea nevoie de operații mai puțin invazive sau vor avea un esofag care funcționează mai aproape de normal.
Pentru asociațiile de pacienți și medici, acest studiu oferă argumente pentru a miza pe o monitorizare pe termen lung și pe colectarea de date. Cu cât problemele actuale după reconstrucția esofagului sunt mai bine identificate, cu atât testele clinice viitoare pot fi concepute și evaluate mai precis.
Cei care se confruntă personal sau în mediul lor cu anomalii congenitale sau cancer esofagian pot întreba medicul curant cum se pregătesc spitalele pentru noile tehnici regenerative. Adesea, există deja studii mai mici cu metode similare, de exemplu pentru piele, cartilaj sau vase de sânge. Acest tip de inițiative constituie un pas către organele complexe la care se lucrează acum în Londra.